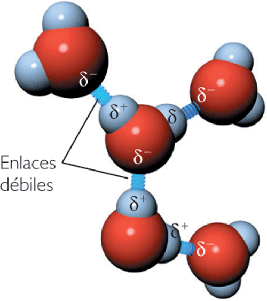
El valor del puente de hidrógeno
Muchas veces no nos paramos a pensar la importancia de la química en nuestro día día. Simplemente asumimos que los fenómenos se producen de una u otra manera sin pensar en su base científica, o más concretamente sin reparar en su base química.
Es el caso por ejemplo de que exista vida en la Tierra. Cuando nos planteamos porqué se dio esta "casualidad" siempre recurrimos a una explicación desde una visión espacial: una estrella de tales categorías, tal proximidad a esa estrella, una atmósfera determinada... Hacemos referencia también a la presencia de agua, pero no reparamos en porqué es tan importante: su estructura.
Debido a la polaridad que existe en las moléculas de agua, aparece entre ellas lo que denominamos una fuerza intermolecular, esto es, una fuerza que se da entre moléculas, una especie de débil enlace. Eso sí, por muy insignificante que sea en comparación con un enlace propiamente dicho, este "enlace", el puente de hidrógeno, es lo que define que la vida exista como tal.
El enlace de puente hidrógeno aumenta muchísimo el punto de ebullición y fusión del agua, tanto que si no existiera, el agua se fundiría a -100ºC y se tornaría gas a -90ºC. Esto es, que si no existieran puentes de hidrógeno no habría agua líquida en la tierra.
Y por otro lado, el puente de hidrógeno torna la estructura del agua en algo complejo y denso, un hecho que permite que el agua líquida donde se forman los puentes, sea más densa que al agua sólida, es decir, que el hielo flote en el agua. Algo que puede parecer insignificante, pero determina que la vida no se frene en los océanos a pesar de que la superficie esté helada.
Así que, valoremos el papel que tiene el puente de hidrógeno en nuestras vidas. Sin él, no existiríamos...